De schimmel die verantwoordelijk wordt gehouden voor de ‘vloek van de mummie’ van Toetanchamon zou binnenkort wel eens een krachtig nieuw wapen tegen leukemie kunnen worden.
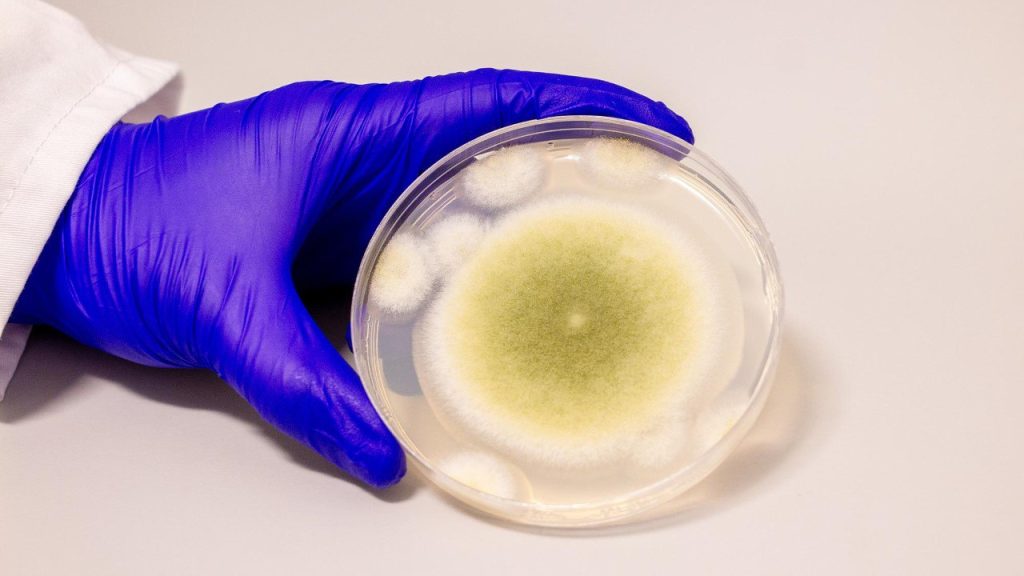
Nadat er in de jaren twintig van de vorige eeuw verschillende mensen voortijdig waren overleden die de tombe van Toetanchamon hadden opgegraven, begonnen geruchten over een mummievloek de ronde te doen. Toen er in de jaren zeventig opnieuw meerdere sterfgevallen volgens hetzelfde patroon plaatsvonden – tien wetenschappers stierven na het betreden van de tombe van Casimir IV in Polen – vonden onderzoekers sporen van Aspergillus flavus, een giftige schimmelspore die longinfecties kan veroorzaken. Wetenschappers vermoeden dat de schimmel ook een rol heeft gespeeld bij de plotselinge sterfgevallen na een bezoek aan het graf van Toetanchamon.
Hoewel schimmels giftig kunnen zijn, maken we er al bijna 100 jaar antibiotica van, zoals penicilline, dat wordt gewonnen uit de schimmel Penicillium. En nu zou de schimmel die vele wetenschappers het leven heeft gekost en geruchten over een mummievloek heeft doen ontstaan, wel eens een krachtig middel tegen kanker kunnen worden.
Een recent onderzoek gepubliceerd in Nature Chemical Biology heeft aangetoond dat bepaalde geïsoleerde verbindingen uit de schimmel A. flavus, ribosomaal gesynthetiseerde en posttranslationeel gemodificeerde peptiden (RiPP’s) genaamd, succesvol kunnen zijn in het aanvallen en vernietigen van leukemiecellen.
Hoewel duizenden RiPP’s uit bacteriën zijn geïsoleerd en beschreven, is slechts een klein aantal RiPP’s uit schimmels gekarakteriseerd. Peptiden bestaan uit twee of meer aminozuren die door chemische bindingen met elkaar zijn verbonden. Aminozuren zijn de bouwstenen die de cel gebruikt om eiwitten te synthetiseren. In wezen kun je RiPP’s zien als minieiwitten, legt José Larios, M.D., transplantatiehematoloog aan het Barbara Ann Karmanos Cancer Institute in Detroit, uit.
Na het zuiveren van vier verschillende RiPP’s ontdekten onderzoekers dat de moleculen een unieke structuur van in elkaar grijpende ringen vormden, die ze ‘asperigimycines’ noemden, naar de schimmel waarin ze werden gevonden. Deze unieke structuur verstoort waarschijnlijk het proces van celdeling. Bovendien presteerde een variant van de RiPP, waaraan onderzoekers een lipide hadden toegevoegd, even goed als de huidige door de FDA goedgekeurde geneesmiddelen cytarabine en daunorubicine voor de behandeling van leukemie.
“Kankercellen delen zich op ongecontroleerde wijze. Deze verbindingen blokkeren de vorming van microtubuli, die essentieel zijn voor de celdeling”, aldus senior auteur Sherry Gao, Ph.D., in een persbericht.
Wanneer natuurlijke celdood niet plaatsvindt en oude of beschadigde cellen zich op ongecontroleerde wijze vermenigvuldigen, kan dit kanker veroorzaken. De nieuwe verbinding die onderzoekers hebben ontdekt, valt kankercellen aan door een cruciale stap in de celvermenigvuldiging te verstoren, aldus Larios. Wanneer een cel zich voortplant, kopieert deze eerst al het genetisch materiaal dat bekend staat als DNA. Zodra het DNA is gekopieerd, moeten de gedupliceerde chromosomen naar tegenovergestelde uiteinden van de cel migreren, een proces dat wordt vergemakkelijkt door microtubuli, of eiwitten in de cel. Het onderzoek suggereert dat deze nieuwe RiPP-verbinding uit schimmels de organisatie van microtubuli verstoort, wat zou leiden tot een defecte chromosoomsegregatie en vervolgens tot celdood, wat nodig is om kanker te behandelen. Dit mechanisme is vergelijkbaar met andere microtubule-remmers die al in gebruik zijn.
Onderzoekers ontdekten dat de verbindingen weliswaar effectief waren tegen leukemiecellen, maar weinig tot geen effect hadden op borst-, lever- of longkankercellen.
“Als oncoloog die leukemie behandelt, ben ik enthousiast over de ontdekking van een potentieel nieuwe cytotoxische verbinding”, zegt Larios. “Alle nieuwe, potentieel therapeutische verbindingen hebben echter een lange en rigoureuze weg te gaan.”
Hoewel deze veelbelovende behandeling ons een nieuwe manier kan bieden om kanker te bestrijden, is het zeker niet de eerste keer dat schimmels in de medische wereld worden gebruikt.
“Het onderzoek naar schimmels om medicijnen te kunnen ontwikkelen is een gevestigde discipline”, legt Larry Norton, M.D., senior vicepresident van het Memorial Sloan Kettering Cancer Center in New York City, uit. Het begon met penicilline en er zijn veel andere antibiotica die zijn afgeleid van schimmels, zegt hij. Er is ook een klasse geneesmiddelen die cefalosporines worden genoemd en die worden gebruikt om bacteriële infecties te behandelen. En statines, die dodelijk zijn voor andere schimmels, worden gebruikt om het cholesterolgehalte te verlagen en het risico op een hartaanval en beroerte bij mensen te verminderen. Daarnaast zijn er enkele schimmels die daadwerkelijk kankerbestrijdende eigenschappen hebben. Er is er een die een enzym genaamd PI3-kinase verstoort, dat erg belangrijk is voor de resistentie tegen medicijnen bij hormoongevoelige kankers zoals borstkanker, aldus Norton.
Leukemie zou natuurlijk niet rechtstreeks worden behandeld met de potentieel dodelijke schimmel, maar met een chemische stof die uit de schimmel wordt gewonnen, aldus Norton. Maar als voor het medicijn een schimmel moet worden gekweekt en de chemische stof vervolgens uit die schimmel moet worden gehaald, vooral op grote schaal (wat nodig zou zijn als de behandeling wordt goedgekeurd), wordt het een zeer dure aangelegenheid.
“Als je chemische stoffen hebt die afkomstig zijn van schimmels of planten, zoeken we naar manieren om ze te synthetiseren of kunstmatig te maken, zodat ze in voldoende zuiverheid en in voldoende hoeveelheid kunnen worden geproduceerd om als medicijn te kunnen worden gebruikt”, zegt Norton.
Voordat deze behandeling kan worden goedgekeurd, moet ze een lang proces doorlopen; de gemiddelde tijd tussen de ontdekking en de goedkeuring door de FDA bedraagt tien jaar, zegt Larios. De nieuwe verbinding moet worden getest in preklinische modellen, waaronder cellijnen en dierproeven, om de werkzaamheid, de juiste dosering en mogelijke bijwerkingen te bepalen. Als deze proeven effectief blijken, volgt een fase I-klinische proef om de veiligheid voor gebruik bij mensen te testen. Vervolgens moet de behandeling meerdere fasen van klinische proeven bij mensen doorlopen voordat de FDA-goedkeuring wordt verkregen. Bovendien moet de verbinding, zoals Norton vermeldt, ook op grote schaal kunnen worden gesynthetiseerd.
Volgens een studie die eerder dit jaar is gepubliceerd in het Journal of the National Cancer Institute, krijgt slechts ongeveer 10 procent van de geneesmiddelen die fase II van de proeven bereiken, uiteindelijk goedkeuring van de FDA. De RiPP’s die in deze studie worden gepresenteerd, hebben dus nog een lange weg te gaan voordat ze mogelijk kunnen worden gebruikt voor de behandeling van leukemie bij patiënten.
Omdat kankercellen bekend staan om hun onstabiele genoom en snelle verdubbelingstijd, waardoor ze zich gemakkelijk kunnen ontwikkelen en resistentie tegen bestaande behandelingen en therapieën kunnen opbouwen, is het voor de kankerbehandeling van groot belang dat er alternatieve behandelingen in het verschiet liggen.
“Hoewel sommige vormen van kanker met vroege opsporing of zelfs een beperkt aantal behandelingscycli kunnen worden genezen, vinden veel kankers uiteindelijk manieren om onze huidige medicijnen te weerstaan”, zegt Larios. “Elke nieuwe behandelingsmethode voor kanker is altijd spannend en hoopgevend voor patiënten die aan kanker lijden.”





